Полина Н. Болоцкова², Елена В. Бондарчук, Валерий Г. Грязнов³, Сергей В. Гудков² ⁴ ⁵, Валерий А. Козлов², Мария А. Окунева¹ ², Олег В. Овчинников³, Олег П. Смолий³, Игорь Ф. Турканов³, Николай Ф. Бункин¹ ².¹ Московский государственный технический университет имени Н.Э. Баумана, 105005, Россия, Москва, ул. 2-я Бауманская. 5;
² Институт общей физики им. А.М. Прохорова. РАН, 119991, Россия, Москва, ул. Вавилова 38;
³ «Концерн ГРАНИТ», 119019, Россия, Москва, Гоголевский проезд 31 кор. 1;
⁴ Нижегородский государственный университет им. Н.И. Лобачевского, 603950, Россия, Нижний Новогород, проспект Гагарина 23;
⁵ Всероссийский научно-исследовательский институт фитопатологии, 143050, Россия, Московская область, Большие Вяземы, ул. Институт 5.Статья опубликована в журнале Polymers (рейтинг — Q1) 29 апреля 2021.
Ссылка на статью на английском

АННОТАЦИЯ
Методом фотолюминесцентной спектроскопии исследовано набухание полимерной мембраны Нафион в деионизированной воде и изотонических растворах NaCl и Рингера. Согласно нашим предыдущим исследованиям, поверхность этой мембраны можно рассматривать как модель клеточной поверхности. Жидкие образцы, которыми пропитывалась мембрана, подвергались предварительной электромагнитной обработке, которая заключалась в облучении этих образцов электрическими прямоугольными импульсами длительностью 1 мкс с помощью погруженных в жидкость платиновых электродов.
Использовалась серия импульсов с частотой следования 11 — 125 Гц; амплитуды импульсов составляли 100 и 500 мВ. Оказалось, что при определенных частотах следования импульсов и их амплитудах характерное время набухания полимерной мембраны существенно отличается от времени набухания в необработанных (контрольных) образцах. В то же время определенные частоты/амплитуды импульсов никакого влияния не оказывают. Временной интервал между электромагнитной обработкой и измерениями составлял около 20 минут. Таким образом, в наших экспериментах проявляются эффекты, связанные с длительной релаксацией жидкостей в ответ на электромагнитную обработку. Эффект длительной релаксации связан с изменением геометрических характеристик бабстонных кластеров при электромагнитной обработке.
1. ВВЕДЕНИЕ
Изучение взаимодействия неионизирующих электромагнитных волн с целыми организмами и, в частности, с хорошо охарактеризованными модельными клеточными системами invitro, получило все большее признание: сообщалось о растущем числе экспериментальных результатов, а также были обнаружены гипотетические механизмы, которые могут способствовать возникновению этих эффектов (см. обзор [1 — 8]).
В то же время значительный интерес представляют исследования взаимодействия низкочастотного диапазона с клеточными структурами. Особенно интересно импульсное низкочастотное воздействие на живые организмы. Например, в недавней работе [9] было показано, что низкочастотное (7 Гц) импульсное электромагнитное поле вызывает гибель клеток в нативных пролиферирующих клетках у достаточно широкой выборки пациентов. В заключение этого раздела отметим, что низкочастотное электромагнитное воздействие оказывает терапевтический эффект, см. Таблицу 2 в недавнем обзоре [8].
Как следует из вышеприведенного обзора, воздействие электромагнитного излучения на биологические системы проявляются на клеточном уровне; большинство экспериментов проводилось на суспензиях клеток в изотонических растворах. В этой связи следует отметить, что некоторые полимерные мембраны и клеточные мембраны обладают схожими свойствами. В частности, в нашей недавней работе [10] было показано, что когда полимерная мембрана Nafion™ набухает в воде, полимерные волокна «раскручиваются» в объем воды. Важно, что эти волокна не отрываются полностью от поверхности раздела мембраны, т. е. вблизи границы образуется «щеточная» структура. Кроме того, при набухании нафиона в воде образуется сеть сквозных каналов в толще мембраны (подробнее см. обзор [11]). Наличие таких каналов нашло применение в ряде практических приложений. Например, процессы переноса жидкости через капиллярную сеть таких каналов широко изучаются с учетом их фрактальных свойств и шероховатости поверхности мембраны, см., например, [12, 13].
Важным параметром топливных элементов на основе нафиона является скорость набухания мембраны в воде. В этой связи необходимо упомянуть работу [14], в которой сложные среды, состоящие из молекул воды в гидрофильных каналах нафиона, изучались методом сверхбыстрой инфракрасной спектроскопии накачки-зондирования. Измерения динамической анизотропии показали, что ориентационные движения молекул воды в каналах нафиона значительно медленнее, чем в объеме воды, и что более низкие уровни гидратации приводят к более медленной ориентационной релаксации. Такое поведение было проанализировано с использованием модели, основанной на ограниченной ориентационной диффузии в конфигурации водородных связей с последующей полной переориентацией посредством прыжковой диффузии.
Учитывая, что мембрана «украшена» размотанными полимерными волокнами, мы приходим к аналогии с клеточной мембраной. Действительно, структура каналов в объеме полимера подобна (условно) липидному бислою клеточной мембраны, в то время как внешняя структура полимерных волокон подобна гликокаликсу (внеклеточный матрикс, см. [15]). Эта аналогия была развита на качественном уровне в нашей недавней работе [16]; в рамках подхода, основанного на этой аналогии, объяснен ряд особенностей, проявляющихся при набухании полимерных мембран в воде и водных растворах солей. Поэтому возникает естественный интерес к исследованию специфического взаимодействия нафиона с деионизированной водой и различными изотоническими растворами, которые подвергались низкочастотному электромагнитному облучению.
Как показано в [16], ряд эффектов, связанных с набуханием мембраны Нафион в воде и водных растворах солей (в [16] водные растворы NaCl исследовались в широком диапазоне концентраций), обусловлен наличием фазы нанопузырьков в воде и водных растворах электролитов (подробнее см. ниже раздел «Обсуждение»). Кроме того, в работе [16] было обнаружено, что кинетика набухания мембраны Nafion™ имеет длительный релаксационный эффект. А именно, эффективное встряхивание жидкого образца (деионизированной воды) приводит к изменению кинетики набухания мембраны, и этот эффект имеет значительное время релаксации (около суток).
Настоящая работа посвящена изучению эффектов длительной релаксации в воде и водных растворах солей, возникающих в результате обработки жидких образцов электромагнитными импульсами с различной частотой и амплитудой следования импульсов.
2. МАТЕРИАЛЫ И МЕТОДЫ
2.1. МАТЕРИАЛЫ
Полимерная мембрана Нафион (C₇HF₁₃O₅S × C₂F₄) представляет собой фторполимер-сополимер на основе сульфированного тетрафторэтилена. Полимерная матрица состоит из тетрафторэтиленовой основной цепи, в которой группы перфторвинилового эфира оканчиваются сульфонатными группами HSO₃. Были исследованы пластины NafionN117 (SigmaAldrich, США) толщиной L₀ = 175 мкм. Пластины Нафион замачивали в воде Milli-Q с удельным сопротивлением 4 МОм × см (измерения проводили через 1 час после приготовления), в изотонических растворах NaCl (0,9%; Мосфарм, Россия) и Рингера (Medpolymer, Россия). В нашем конкретном случае раствор Рингера состоял из NaCl (8,6 г/л), KCl (0,3 г/л) и CaCl₂ × 6H₂O(0,25 г/л), растворенных в воде.
2.2. ИНСТРУМЕНТЫ
2.2.1. Фотолюминесцентное исследование
В этом подразделе мы кратко опишем экспериментальный протокол, более подробно см. [10]. Методика эксперимента основана на возбуждении фотолюминесценции с поверхности нафиона накачкой в УФ-диапазоне. Для возбуждения люминесценции необходимо облучить вещество в пределах одной из полос поглощения. Некоторые замечания, относящиеся к данному вопросу, следующие: известно [17], что один из максимумов поглощающей способности как сухого, так и набухшего в воде нафиона происходит на длине волны = 270 нм. Также известно (см., например, [18]), что вода в этом спектральном диапазоне не поглощает. Дополнительно отметим, что когда оптическое излучение взаимодействует с веществом, и внутри полосы поглощения облучается сложная молекулярная система, квантовые переходы стимулируются в более длинноволновом диапазоне, т.е. должна возникать фотолюминесценция.
Настоящая работа посвящена изучению взаимодействия мембраны Нафион с жидкими образцами, обработанными электрическими импульсами с низкой частотой повторения, фотолюминесцентными методами, которые широко используются в исследованиях полимеров, см., например, [19 — 23]. В наших экспериментах по фотолюминесценции мы использовали излучение с длиной волны λ = 369 нм, соответствующей длинноволновой области полосы поглощения. В параллельных экспериментах (см. [10]) было обнаружено, что концевые сульфогруппы HSO₃ служат центрами люминесценции нафиона при УФ-облучении.
На рис. 1 представлена зависимость люминесцентного сигнала Pот раствора нафиона в изопропаноле на длине волны λ = 460 нм (спектральный максимум люминесценции); нулевая абсцисса соответствует чистому изопропанолу. Концентрация раствора в этом случае нам не известна; считаем (условно), что концентрация составляет 100 е.п. сразу после извлечения пластины Нафион из раствора, а затем раствор пропорционально разбавляли изопропиловым спиртом.
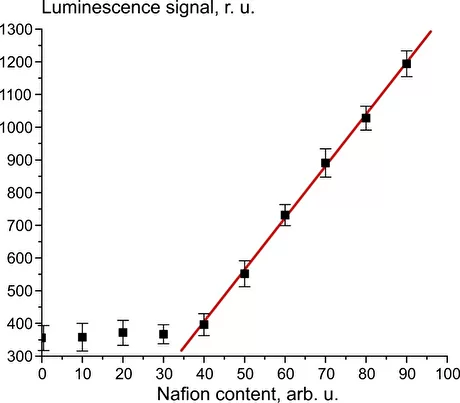
Рис. 1. Зависимость люминесцентного сигнала P от содержания нафиона в растворе изопропанола. Отрезок прямой на рис.1 можно выразить формулой
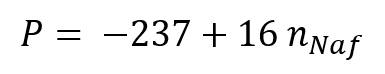
(1)где nNaf — объемная плотность числа центров люминесценции, т.е. концевых сульфогрупп. Поскольку эти группы присоединены к полимерным цепям, nNafможно связать с объемной плотностью числа частиц нафиона. Полученную зависимость можно представить в виде
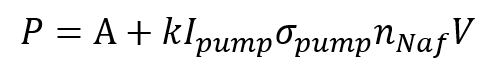
(2)где Ipump— интенсивность накачки, A = 20 — 270 отн. ед. соответствует спектральной плотности шума мини-спектрометра и посторонней засветки, k— коэффициент передачи установки, V— объем люминесценции, slum— сечение люминесценции (очевидно, что спектральный максимум slum соответствует l = 460 нм). Из рис. 1 следует, что slum= постоянная величина.
Для проведения экспериментов по спектроскопии фотолюминесценции была разработана и смонтирована установка для спектроскопии фотолюминесценции в геометрии скользящего падения (подробнее см. [10]). Схема экспериментальной установки представлена на рис.2.Зондирующее излучение лазерного диода непрерывного действия (1) (оптическая накачка) на длине волны λ= 369 нм вводилось в многомодовое кварцевое оптическое волокно (2) диаметром Ø = 100 мкм и числовой апертурой NA = n × sin α = 0,3, где n = 1 — показатель преломления воздуха, α — угол расхождения луча на выходном конце волокна в воздухе.
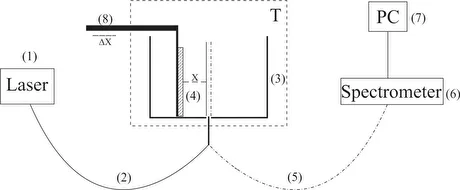
Рис. 2. Схема экспериментальной установки для проведения лазерной люминесцентной спектроскопии.
Волокно закреплялось в отверстии, расположенном в центре дна цилиндрической кюветы (3) из нержавеющей стали; направление пучка накачки задает оптическую ось экспериментальной установки. Кювету термостабилизировали при комнатной температуре (T = 23 °C) с точностью до ± 0,1 °C и заполняли исследуемым жидким образцом. Исследовалось набухание квадратной пластины нафиона (4) со стороной h = 4 мм и толщиной d = 175 мкм.
Пластина закреплялась параллельно оптической оси, т.е. эксперименты проводились при скользящем падении. Вертикальные края пластины нафиона жестко фиксировались двумя вертикальными параллельными зажимами параллельно оптической оси; т.е. эксперименты проводились при скользящем падении; дополнительный субстрат для фиксации пластины не использовался. Размер зажимов был намного меньше ширины пластины Нафион; т.е. для центральной области пластины в вертикальном направлении (эта область подвергалась облучению УФ-накачкой) реализованы приблизительные условия свободного края.
В начале эксперимента сухая (безводная) пластина нафиона фиксировалась в пустой кювете; пластину можно перемещать по горизонтали с помощью шагового двигателя (8), тем самым изменяя положение пластины по отношению к оптической оси. При этом был достигнут максимум сигнала люминесценции; соответствующее положение пластины нафиона относительно оптической оси считается оптимальным.
При заливке жидкого образца в кювету первоначально гидрофобная пластина нафиона изгибалась вдоль оптической оси. Однако такой изгиб приводил только к эффективному смещению границы нафион-вода (это смещение составляло около 1 мм), но не приводил к изменению угла падения излучения накачки. Для восстановления оптимального положения пластины относительно оптической оси проводилась дополнительная юстировка с помощью шагового двигателя (8). Люминесцентное излучение отражалось внутренней поверхностью кюветы (нафион прозрачен в видимом диапазоне) и собиралось вдоль оптической оси кюветы. Это привело к значительному увеличению интенсивности люминесценции.
Сигнал люминесценции принимался кварцевым волокном (5), закрепленным в центре кюветы, и передавался на миниспектрометр (6) ФСД-8 (Россия). Экспериментальные данные собирались компьютером (7). В эксперименте исследовалась временная динамика интенсивности люминесценции в спектральном максимуме в зависимости от времени пропитывания пластинки нафиона в исследуемой жидкости. Начало отсчета времени выдержки соответствует моменту заливки жидкого образца в кювету.
2.2.2. Обработка жидких образцов
Для изучения воздействия электромагнитной обработки на исследуемые жидкости была разработана экспериментальная установка, которая позволяла подвергать жидкие образцы воздействию электрических импульсов положительной/отрицательной полярности с частотой повторения в диапазоне 5 — 125 Гц с возможностью варьирования амплитуды и длительности импульсов. В экспериментах использовались генератор импульсов Г5-63 (Россия) и осциллограф АКИП 4115/3А (Россия).
Образцы исследуемой жидкости переливали в кювету объемом 5 мл. Затем в кювету погружали платиновые электроды, подключенные к генератору импульсов; расстояние между электродами составляло 5 мм, площадь электродов в жидкости была 10 мм². Использовались импульсы длительностью мкс и с амплитудами 100 и 500 мВ (данные по напряжению снимались после погружения электродов в жидкий образец). Жидкие образцы подвергались воздействию электрических импульсов в течение 20 минут (время обработки). Типичные импульсы, использованные в нашем эксперименте, показаны на рис. 3: панель (а) — 100 мВ и панель (б) — 500 мВ; частота следования импульсов указана в правом нижнем углу.
Электрохимический потенциал платины в соответствии с реакцией Pt²⁺ + 2e ⁻ ⇌ Pt(s) составляет ϕ₀ = +1,2 В, см. [24]; очевидно, что напряжение импульсов, подаваемых на электроды, не должно превышать значения ϕ₀, чтобы избежать электрохимических реакций на электродах. Чтобы убедиться, что мы не имеем дело с электрохимическими реакциями, мы контролировали pH исследуемых жидкостей до и после электромагнитной обработки. Для этого использовался pH-метр HANNAHI 98108 PHep + (США), калиброванный по стандартным кислотным и щелочным титрам, имеющим pH = 4,06 и 9,18 соответственно. Оказалось, что электромагнитная обработка не привела к изменению pH: до и после обработки для деионизированной воды pH = 5,7 ±0,1, для раствора NaClpH = 6,2 ± 0,1, для раствора Рингера = 5,5 ±0,1.
3а3б
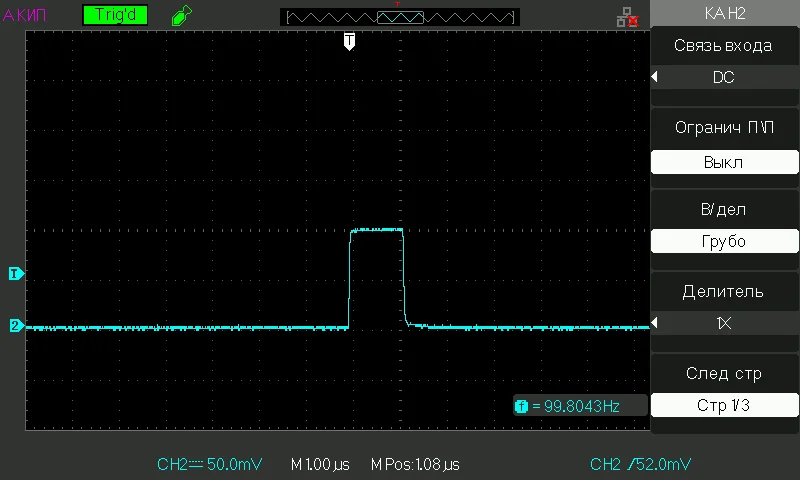
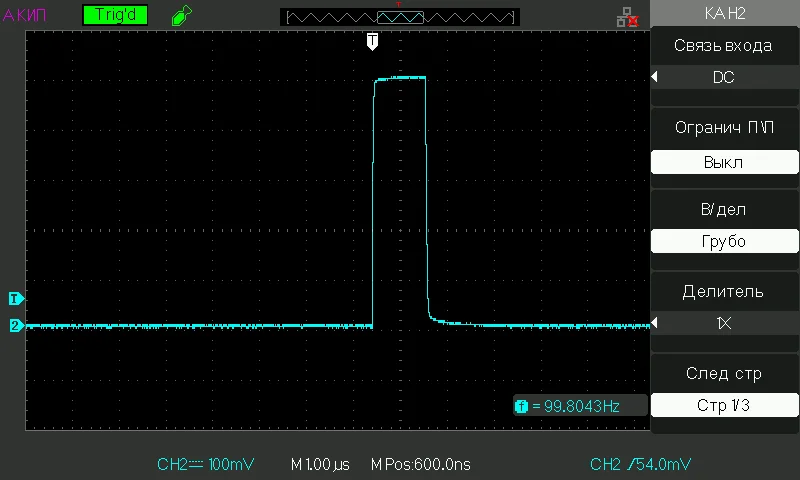
Рис. 3. Осциллограммы импульсов, использованных в эксперименте; частота следования f указана в правом нижнем углу (в данном конкретном случае f= 100 Гц). Панель (а) — 100 мВ. Панель (б) — 500 мВ.
3. ЭКСПЕРИМЕНТАЛЬНЫЕ РЕЗУЛЬТАТЫ
Представленные ниже зависимости интенсивности люминесценции в спектральном максимуме от времени набухания полимерной мембраны соответствуют усреднению по пяти последовательным измерениям. Доверительные интервалы указаны на всех графиках, см. ниже.
Сначала мы измерили интенсивность люминесценции в спектральном максимуме (460 нм) в зависимости от времени выдержки для необработанных (контрольных) образцов деионизированной воды после отстаивания в течение часа в колбе, открытой для атмосферной среды, а также необработанных (референтных) образцов изотонического раствора NaCl и раствора Рингера. На рис. 4 (а) показана зависимость интенсивности фотолюминесценции от времени в спектральном максимуме (460 нм) для деионизованной воды и раствора NaCl. На рис. 4 (б) представлена зависимость интенсивности фотолюминесценции раствора Рингера от времени. Видно, что для всех жидкостей экспериментальные точки расположены примерно на одних экспоненциальных кривых.
Соответствующие формулы приведены на вставках и выделены разными цветами: синим цветом для воды и красным цветом для раствора NaCl. Как следует из рис. 4 (а), время затухания экспоненциальной функции для деионизованной воды и раствора NaCl одинаково и равно τ₀ = 14,3 мин, а для раствора Рингера (рис. 4 (б) равно τ₀ = 12,3 мин. Предэкспоненциальные множители и свободные константы для данных экспонент также незначительно различаются. Таким образом, для необработанной деионизированной воды и изотонических солевых растворов временные зависимости интенсивности люминесценции хорошо выражаются очень близкими убывающими экспоненциальными функциями, т.е. ионные добавки вряд ли повлияют на динамику набухания Нафиона.
4а4б
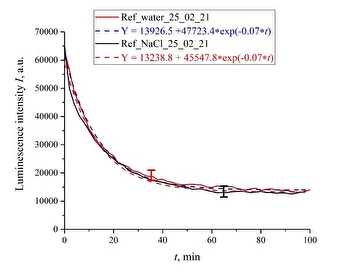
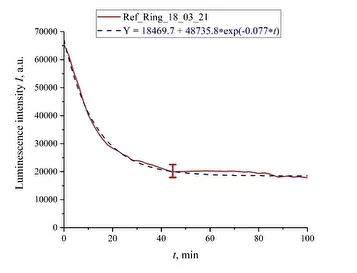
Рис. 4. Интенсивность люминесценции в спектральном максимуме в зависимости от времени пропитывания полимерной мембраны для необработанных растворов (контрольные образцы); (а) — деионизированная вода; (б) — раствор NaCl;
(в) — раствор Рингера.
Интервал времени между окончанием электромагнитной обработки жидких образцов и началом измерения интенсивности фотолюминесценции составил 10 минут. Этот интервал включал первоначальную юстировку установки для спектроскопии фотолюминесценции с последующим заливанием обработанной жидкости в кювету, показанную на рис.2.
Чтобы не загромождать статью, мы приводим только наиболее характерные зависимости интенсивности люминесценции от времени пропитывания полимерной мембраны. На рис. 5 представлена зависимость для раствора Рингера, обработанного импульсами с амплитудой 100 мВ и частотой следования 20 Гц. На этом же рисунке показана зависимость для контрольного образца. Видно, что обе зависимости хорошо описываются убывающими экспоненциальными функциями, но для обработанного образца время затухания примерно в два раза меньше.
На этом же графике показаны расчеты коэффициента ранговой корреляции Пирсона для полученных зависимостей. Значение коэффициента ранговой корреляции (~ 0,9) показывает, что в обоих случаях мы, по-видимому, имеем дело с процессом, имеющим одинаковую физическую природу, но кинетические характеристики этого процесса различаются после обработки электрическими импульсами. Обратите внимание, что полученные графики были усреднены по пяти последовательным зависимостям: графики показывают доверительный интервал для точек, полученных путем усреднения полученных путем усреднения.
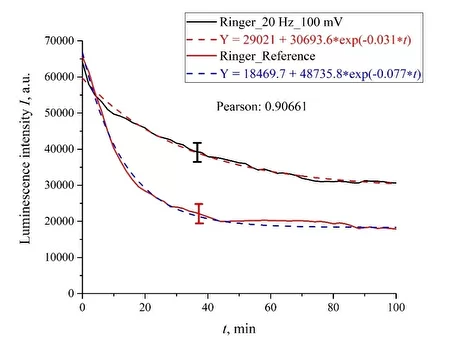
Рис. 5. Результаты обработки импульсами амплитудой 100 мВ при частоте следования 20 Гц: для раствора Рингера.
На рис. 6 представлена зависимость для раствора Рингера, обработанного импульсами с амплитудой 100 мВ и частотой следования 125 Гц; здесь же показана зависимость для контрольного образца. Видно, что обе зависимости также хорошо выражаются убывающими экспоненциальными функциями, но для обработанного образца время затухания примерно вдвое больше.
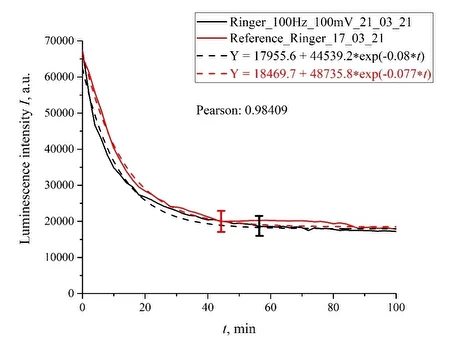
Рис. 6. Результаты обработки импульсами амплитудой 125 мВ при частоте следования 500 Гц: для раствора Рингера.
На рис. 7 представлена зависимость для раствора Рингера, обработанного импульсами с амплитудой 100 мВ и частотой следования 100 Гц. На этом же графике показана зависимость для контрольного образца. Видно, что обе зависимости хорошо выражаются убывающими экспоненциальными функциями и примерно совпадают.
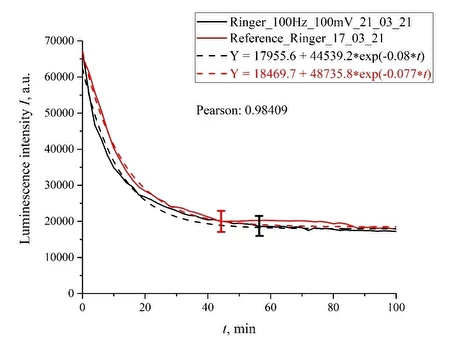
Рис. 7. Результаты обработки импульсами амплитудой 100 мВ при частоте следования 100 Гц для раствора Рингера.
Как следует из этих графиков, после обработки электрическими импульсами время затухания экспоненциальных функций, используемых для выражения экспериментальных зависимостей, может увеличиваться/уменьшаться по сравнению с эталонными зависимостями или может не изменяться вовсе.
Результаты проведенных экспериментов суммированы на рис.8, где представлены зависимости τ/τ₀, где τ/τ₀ — время затухания эталонной зависимости, τ — время затухания соответствующей зависимости после обработки от частоты следования импульсов для деионизированной воды (панель (а)), изотонического раствора NaCl (панель (b)) и раствора Рингера (панель (с)); черные кривые соответствуют амплитуде импульса 100 мВ, а красные кривые соответствуют амплитуде импульса 500 мВ. Видно, что полученные зависимости качественно коррелируют между собой для всех исследованных жидкостей. 8а8б 8в
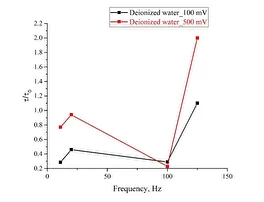
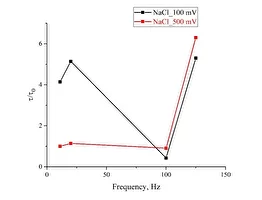
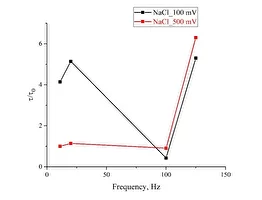
Рис. 8. Зависимость t/t0от частоты следования импульсов для амплитуд импульсов 100 мВ (черная кривая) и 500 мВ (красная кривая); (а) — деионизированная вода; (б) — раствор NaCl; (c) — раствор Рингера
4. ОБСУЖДЕНИЕ
Как следует из графика интенсивности люминесценции в спектральном максимуме на рис.1 (см. также формулу (1)), динамика интенсивности люминесценции I полностью контролируется объемной плотностью числа центров люминесценции nNaf (сульфогрупп в данном случае, см. [27]), сечением люминесценции σlum и объемом люминесценции V. Объемную плотность центров люминесценции в объеме V можно представить как nNaf = C/V, где C — общее количество полимерных частиц в объеме V.
Очевидно, этот объем определяется поперечным сечением лазерного луча в приповерхностном слое пластины Нафион (напомним, что мы облучаем пластину в геометрии скользящего падения) и высотой пластины, т. е. объем Vфиксирован. Поскольку при набухании молекулы воды проникают в поверхностный слой мембраны, значение nNafвнутри этого слоя должно уменьшаться. Тогда при предположении, что σlum является постоянным значением (заметим, что нет оснований предполагать, что σlum изменяется при набухании), единственным параметром, зависящим от времени, является объемная плотность центров люминесценции nNaf.
Вводя характерное время затухания τ, которое соответствует времени набухания, мы получаем дифференциальное уравнение
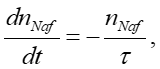
(3)т.е.
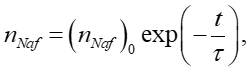
(4)где (nNaf)₀ — объемная плотность центров люминесценции при t = 0 (т.е. в сухом нафионе). Как следует из приведенных выше экспериментальных графиков, обработка электрическими импульсами приводит к изменению времени набухания.
Как было указано выше, коэффициент ранговой корреляции Пирсона между контрольным и обработанным жидкими образцами близок к единице. На наш взгляд, это косвенно свидетельствует о том, что сечение люминесценции lum не изменяется в результате обработки, то есть динамика набухания мембраны для обработанных и необработанных образцов описывается экспоненциальной функцией (4). Очень важно, что для контрольных образцов экспоненциальные функции, описывающие динамику набухания, практически совпадают, см. рис. 4. В то же время, как видно из графиков на рис. 8, характерное время набухания t изменяется после обработки электрическими импульсами.
Как видно из графиков, отношение τ/τ₀ для разных отсчетов существенно зависит от частоты следования и амплитуды импульсов.
Например, для изотонического раствора NaCl (панель (б)) обработка на частотах 11 и 20 Гц для амплитуды импульса 100 мВ приводит к значительному увеличению скорости набухания полимерной мембраны, а для амплитуды импульса 500 мВ скорость набухания меняется очень незначительно по сравнению с контрольным образцом.
Отметим также, что наиболее значительное увеличение скорости набухания наблюдается также для изотонического раствора NaCl при частоте следования 125 Гц для обеих амплитуд импульсов. Интересно отметить, что импульсная обработка деионизированной воды для обеих амплитуд импульсов приводит в первую очередь к замедлению, а не к увеличению скорости набухания (τ/τ₀ ≤ 1); исключение составляет обработка импульсами частоты 125 Гц с амплитудой 500 мВ. Отметим также, что частота 100 Гц выглядит особенной, так как для этой частоты значения τ/τ₀ для 100 и 500 мВ очень близки у всех исследованных образцов. Кроме того, для всех исследованных жидкостей наблюдается увеличение t/t0 в диапазоне 100 — 125 Гц для обеих амплитуд импульсов.
Эти результаты демонстрируют, что обработка жидких образцов по указанному протоколу приводит к значительным изменениям скорости набухания мембраны, а эффект от такой обработки имеет достаточно длительное время релаксации (порядка нескольких десятков минут). Можно предложить следующие механизмы реализации этого эффекта. Во-первых, нельзя полностью исключить возможность появления ионных примесей на платиновых электродах в процессе обработки. Ясно, однако, что в этом случае изменение скорости набухания должно однообразно зависеть от количества подводимой энергии при электролизе, т.е. зависимости τ/τ₀ от частоты следования импульсов (эти зависимости показаны на рис. 13) должны вести себя однообразно. Кроме того, для нас очень важно, что для необработанных образцов деионизованной воды и изотонических растворов NaCl и Рингера время затухания τ₀ совпадает с хорошей точностью. Наконец, для всех исследованных образцов значение pH не меняется до и после обработки.
Таким образом, на наш взгляд, механизм загрязнения можно исключить.
Как известно [25], характерное время процессов релаксации в воде составляет 10⁻¹¹ –10⁻¹² с. Это, во-первых, время жизни водородной связи между молекулами воды; разрыв водородной связи происходит из-за вращательной броуновской диффузии молекул. Во-вторых, это время затухания локальных колебаний давления/плотности.
Полагая, что характерный размер такой флуктуации составляет δ ~ 10 – 100 нм, для времени затухания такой флуктуации получаем оценку t ~ δ/c, где c — скорость звука в воде, т.е. t ~ 10⁻¹¹ – 10⁻¹⁰ с. Таким образом, казалось бы, что процессы с временами релаксации порядка нескольких десятков минут не могут возникнуть в воде и водных растворах электролитов.
Вместе с тем, как показано в ряде работ (см., например, обзор [26] и ссылки в нем), существуют долгоживущие газовые нанопузырьки диаметром 200 — 300 нм в объеме воды и водных солевых растворах при нормальных условиях. Указанный размер обычно наблюдается в экспериментах, основанных на методе динамического рассеяния света, см. [27] для получения более подробной информации. В наших предыдущих работах [28 — 30] было показано, что если жидкость насыщена растворенным газом (например, атмосферным воздухом) и имеет ионную составляющую, то в ней самопроизвольно возникают ионно-стабилизированные газовые нанопузырьки. Стабилизация происходит за счет адсорбции анионов на внутренней (со стороны газовой фазы) поверхности нанопузырьков. Такие нанопузырьки были названы бабстонами (аббревиатура от «пузырьки, стабилизированные ионами»), см. [28].
В этом случае поверхностное натяжение бабстонов полностью уравновешивается отрицательным электростатическим давлением адсорбированных ионов, а давление газа внутри бабстонов оказывается равным атмосферному давлению. Отметим, что недавно была подтверждена модель стабилизации нанопузырьков в объеме жидкости за счет адсорбции ионов на поверхности нанопузырьков, см., например, [31 — 33].
Как следует из исследований [28 — 30], бабстоны устойчивы как механически, так и диффузионно благодаря наличию ионной примеси. Понятно, что ионная составляющая существует в изотонических растворах NaCl и Рингера. Что касается деионизованной воды, то бабстоны стабилизируются за счет адсорбции анионов HCO₃⁻ и CO₃²⁻ на поверхности бабстонов, см. нашу недавнюю работу [34]. Эти анионы возникают из-за диссоциации угольной кислоты, которая, в свою очередь, является результатом гидролиза CO₂ в воде. Возникновение бабстонов происходит из-за кулоновской неустойчивости так называемых «капель ионного конденсата». Ядрами таких капель являются димеры «ион — молекула газа», см. нашу недавнюю работу [35]. В этой же работе, в частности, мы оценили время нуклеации бабстона, которое составляет около 2,4 × 10⁻⁸ с.
При рассмотрении стабилизации бабстонов за счет ионной адсорбции необходимо учитывать, что отрицательно заряженные (из-за адсорбции анионов) газовые ядра бабстонов всегда окружены сферически-симметричным диффузионным облаком противоионов (дебаевское экранирование). Когда бабстоны движутся в вязкой жидкости, периферийные слои этого облака эффективно «размываются», что приводит к образованию ζ-потенциала. В этом случае бабстоны оказываются заряженными отрицательно. Действительно, известно (см., например, [36 — 38]), что при электрофорезе пузырьки движутся к аноду.
Оценим теперь величину смещения бабстонов внутри плоского конденсатора, к которому прикладывается серия электрических импульсов напряжением U= 500 мВ и длительностью τ’ = 1 мкс с частотой следования импульсов 10 Гц. Полагая, что ζ-потенциал j нанопузырьков с радиусом R выражается как
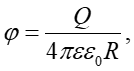
(5)где ε = 80 — диэлектрическая проницаемость воды, и подставив ϕ = -10 мВ (см., например, [33]), и R = 100 нм, получим Q ~ 10⁻¹⁷ C, т.е. около 100 элементарных зарядов. Предположив далее расстояние d между пластинами конденсатора равным 1 см, для напряженности электрического поля внутри конденсатора получим Е = U/(εd) ≈ 0,6 В/м. В случае равномерного движения бабстона, имеющего скорость v, получаем
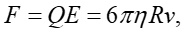
(6)где η = 10⁻³ Па × с — динамическая вязкость воды при комнатной температуре. Таким образом, получаем, что к бабстону приложена сила F = 0,6×10⁻¹⁷ Н, а скорость бабстона v = 0,3×10⁻⁸ м/с, т.е. за время τ’= 1 с пузырек движется на дистанцию ∆l ’ ~ 3×10⁻¹⁵ м. Далее оценим случайное смещение бабстона ∆l ” в результате броуновской диффузии в интервалах τ’; мы получаем
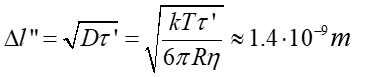
(7)где D — коэффициент броуновской диффузии, Т = 300 К. Видно, что ∆l ” >> ∆l’ , т.е. за импульс длительностью 1 мкс среднее положение отдельного бабстона практически не меняется. Мы не можем представить себе физический механизм процессов со временем релаксации порядка десятков минут, основанный на модели отдельных бабстонов.
Следует отметить, что в водных растворах солей с достаточно высокой концентрацией ионов отдельные бабстоны способны коагулировать друг с другом с образованием бабстонных кластеров размером от 700 нм до 2 мкм. Экспериментальные исследования бабстонных кластеров в водных растворах NaCl, проведенные с динамическим рассеянием света, описаны в [39 — 41]. Как было показано в этих работах, кластерная фаза проявляется при концентрациях ионов > 0,1 М; очевидно, что этому условию удовлетворяют изотонические растворы NaCl и Рингера, тогда как в деионизированной воде концентрация ионов меньше. Действительно, в этой воде значение pH = 5,7 ±0,1 до и после обработки, т.е. содержание ионов составляет ~ 10⁻⁶ М.
Как было установлено в экспериментальной работе [39], объемная плотность бабстонных кластеров в 0,1 М растворе NaCl составляет около 2×10⁵ см⁻³. Зависимость объемной плотности отдельных бабстонов от концентрации ионов в растворе NaCl исследовалась в [29]. В данной работе установлено, что при концентрации ионов 10⁻⁶ М объемная плотность бабстонов составляет ~ 10⁶ см⁻³, а при концентрации 10⁻¹ М (физиологические растворы) — 3×10⁷ см⁻³.
Таким образом, объемные плотности бабстонов/бабстонных кластеров существенно различаются в деионизированной воде и изотонических растворах. Кроме того, кластеры практически не проявляются в экспериментах по динамическому рассеянию света в деионизованной воде. Кроме того, кластеры являются фрактальными объектами; их фрактальные размерности и радиусы инерции в водных растворах NaCl измерены в [29, 39 — 41]. Наконец, характерное время жизни кластеров было измерено в [29]. В этом эксперименте сначала измеряли распределение рассеивателей по размерам в 1 М растворе NaCl, а затем жидкий образец выстаивали в течение 6 месяцев в стационарных условиях в герметичной (без доступа атмосферного воздуха) кювете высотой 2 см. Оказалось, что рассеиватели микронных размеров (бабстонные кластеры) после осаждения исчезают, а субмикронные рассеиватели (отдельные бабстоны) остаются в жидкости («выживают»).
Исчезновение крупных рассеивателей, очевидно, связано с всплыванием кластера с последующим его разрушением на границе раздела жидкости, тогда как отдельные бабстоны обладают нейтральной плавучестью, т.е. не всплывают. Таким образом, можно утверждать, что бабстоны — это равновесная фаза водного раствора электролита при нормальных условиях, а бабстонные кластеры — долгоживущая фаза.
Коагуляция бабстонов и образование кластеров теоретически рассмотрены в [42]. В данной работе распределение Q(r) всего заряда Q₀ газового ядра радиусом R₀ и окружающего газовое ядро облака противоионов (толщина этого облака равна (r — R₀), где радиус-вектор r возникает в бабстонном центре) в солевых растворах с низкой концентрацией ионов является монотонной функцией: Q(r) → 0 для r → ∞ для всех значений r. В то же время при высоких концентрациях ионов функция Q(r) перестает быть монотонной: при некотором значении r = r₀ имеем Q(r₀) = 0 (изоэлектрическая точка), но условие Q(r) → 0 при r → ∞ все еще выполняется. Таким образом, можно говорить об изменении знака функции Q(r) в концентрированных ионных растворах. Этот эффект описан, например, в [43 — 45]; физическая природа этого эффекта связана с зарядом газовой сердцевины Q₀: при малых концентрациях ионов выполняется условие
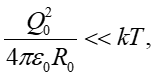
(8)где k — постоянная Больцмана. В то же время при высоких концентрациях ионов условие (8) нарушается:
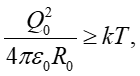
(9)что приводит к эффекту инверсии, см. [43 — 45]. Как показано в [42], при высоких концентрациях ионов мы всегда имеем дело с составными частицами двух типов, имеющими электрические заряды противоположного знака. Эти составные частицы состоят из газового ядра (величина его заряда фиксирована) и облака противоионов, остающегося после смывания периферийных ионных слоев из-за движения в вязкой жидкости. Это приводит к кулоновскому притяжению разноименно заряженных составных частиц с образованием кластеров.
На основе результатов [42] мы модифицировали иерархическую модель кластеризации сферических частиц [46]; подробно иерархическая модель описана в обзоре [47]. В [46] мы численно моделировали рост кластеров, состоящих из сферических мономеров. Серии кластеров генерировались итеративно, начиная с N отдельных сферических частиц. На каждом этапе процесса итерации случайным образом выбирались два кластера, а затем эти кластеры связывались друг с другом со случайной взаимной ориентацией, образуя новый кластер.
Мы нашли решение проблемы обратного рассеяния в виде стохастического ансамбля из 2 × 10³ кластеров иерархического типа, подчиняющихся экспоненциальному распределению p(N) ∼ exp(−αN) по числу N бабстонов в кластере (N ≥ 1, α> 0). Здесь α — параметр модели, учитывающий притяжение частиц при агрегации баллистического типа. В такой иерархической модели кластер-кластерной агрегации средняя фрактальная размерность D ансамблей кластеров монотонно зависит от параметра α. Параметр α можно рассматривать как дополнительную «степень свободы», позволяющую описать экспериментально обнаруженную угловую зависимость элементов индикатрисы рассеяния, см. нашу работу [39]. В данной работе мы рассчитали набор матриц рассеяния как средние значения по случайным кластерным ансамблям со статистическими параметрами, взятыми на единой дискретной сетке. Решение обратной задачи рассеяния было найдено путем минимизации расхождения между измеренными угловыми профилями матрицы рассеяния и такими же профилями.На рис. 9 показан пример таких реализаций для физиологического раствора NaCl; α = −1,4, фрактальная размерность кластера D = 2,45, количество бабстонов в кластере N = 420, радиус бабстона R = 100 нм; эта цифра взята из [39].
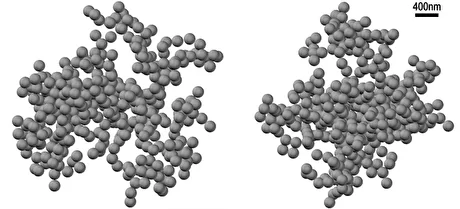
Рис.9. Взаимно перпендикулярные проекции стохастической реализации иерархического бабстонного кластера с параметрами: число бабстонов N = 400, радиус бабстона R = 100 нм, фрактальная размерность D = 2,45, см. [39].
В [46] напряженность электростатического поля, при которой проявляются эффекты коагуляции, предполагается сферически симметричной. Электростатическая сила, приводящая к росту кластера, определяется формулой
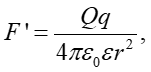
(10)где r — расстояние между центром бабстона с зарядом Q ~ 10⁻¹⁷ С и центром притяжения на поверхности кластера. Пусть этот центр имеет заряд q ; точное значение этого заряда нам неизвестно. Однако без потери общности мы можем положить q ≈ -Q, предполагая, что мы имеем дело с притягивающим взаимодействием. Полагая, что r ~ 1 мкм (характерный радиус кластера), получаем F ’ ~ 10⁻¹⁴ N >> F, где F — сила, приложенная к бабстону в поле плоского конденсатора, см. комментарии к уравнению (6). Однако ясно, что оценка силы F ’ очень приблизительна, поскольку нам неизвестен эффективный заряд q. Видимо, нужен более точный теоретический анализ и новые эксперименты. Эти эксперименты должны включать изучение угловых зависимостей элементов матрицы рассеяния для обработанных/необработанных жидких образцов. Однако ясно, что в отсутствие приложенного импульсного поля агрегация бабстонов и образование кластеров развиваются в центрально-симметричном поле, тогда как при обработке электрическими импульсами агрегация бабстонов происходит в комбинации центрально-симметричного поля и равномерно распределенного поля плоского конденсатора. Таким образом, можно утверждать, что режимы агрегации бабстонов и фрактальные свойства бабстонных кластеров будут разными для обработанных/необработанных образцов. Кроме того, поскольку объемная плотность бабстонных кластеров в деионизованной воде и водных растворах солей различна, эффекты обработки электрическими импульсами для этих жидкостей также должны отличаться друг от друга. Конечно, мы до сих пор не можем прокомментировать, почему изменение геометрических свойств бабстонных кластеров, объемная плотность которых в 0,1 М растворе NaCl не очень велика (~2×10⁵ см⁻³), приводит к изменению скорости набухания. полимерной мембраны. Однако мы полагаем, что эта модель может пролить свет на механизмы долговременной релаксации в воде и водных растворах солей.5. ВЫВОДЫТаким образом, при низкочастотной обработке электрическими импульсами деионизированной воды и изотонических растворов NaCl и Рингера внутренние параметры жидкой матрицы, которые определяют скорость набухания полимерной мембраны Нафион, должны измениться. Эффект может быть связан с изменением геометрических характеристик бабстонных кластеров в процессе обработки. Поскольку бабстонные кластеры представляют собой долгоживущую фазу воды и водных растворов солей, в рамках предложенной модели длительная релаксация жидких образцов после обработки электрическими импульсами находит свое естественное объяснение. Поскольку, согласно нашему предположению, мембрана Нафион похожа на клеточную мембрану, см. [16], электромагнитная обработка может использоваться в биомедицинской практике для приготовления лекарств с переменной скоростью проникновения препарата в клетку/живую ткань.
ЛИТЕРАТУРА
- Adey, W.R. Tissue interactions with nonionizing electromagnetic fields. Physiol. Rev. 1981, 61, 435-514
- Adey, W.R.; Lawrence, A.F. (eds.): Nonlinear Electrodynamics in Biological Systems. Plenum, NewYork 1984.
- Chiabrera, A.; Nicolini, C.; Schwan, H.P. (eds.): Interactions Between Electromagnetic Fields and Cells. Plenum, NewYork 1985.
- Polk, C.; Postow, E.(eds.): CRC Handbook of Biological Effects of Electromagnetic Fields. CRC, BocaRaton 1986.
- Blank, M.; Findl, E.(eds.): Mechanistic Approaches to Interactions of Electromagnetic Fields with Living Systems. Plenum, NewYork 1987.
- Fröhlich, H. (ed.): Biological Coherence and Response to External Stimuli. Springer, Heidelberg 1988.
- Wilson, B.W.; Stevens, R.G.; Anderson, L.E. (eds.): Extremely Low Frequency Electromagnetic Fields: The Question of Cancer. Batelle, Columbus 1991.
- Saliev, T.; Begimbetova, D.; Masoud, A.R.; Matkarimov, B. Biological effects of non-ionizing electromagnetic fields: Two sides of a coin. ProgressinBiophysicsandMolecularBiology 2019, 141, 25-36.
- Kaszuba-Zwoińska, J.; Ćwiklińska, M.; Balwierz, W.; Chorobik, P.; Nowak, B.; Wójcik-Piotrowicz, K.; Ziomber, A.; Malina-Novak, K.; Zaraska, W.; Thor, P.J. Changes in cell death of peripheral blood lymphocytes isolated from children with acute lymphoblastic leukemia upon stimulation with 7 Hz, 30 mT pulsed electromagnetic field, Cellular and Molecular Biology Letters 2015, 20, 130-142.
- Bunkin, N.F.; Shkirin, A.V.; Kozlov, V.A.; Ninham, B.W.; Uspenskaya, E.V.; Gudkov, S.V. Near-surface structure of Nafion in deuterated water. J. Chem. Phys. 2018, 149, 164901.
- Mauritz, K.A.; Moore, R.B. State of understanding of Nafion. Chem. Rev. 2004, 104, 4535-4585.
- Xiao, B.;Zhang, Y.; Wang, Y.;Jiang,G.; Liang, M.; Chen, X.; Long, G. A fractal model for Kozeny–Carman constant and dimensionless permeability of fibrous porous media with roughened surfaces, Fractals 2019, 27, 1950116.
- Ali, A.; Shah, K.; Alrabaiah, H.; Shah, Z.; Rahman, G.U.; Islam, S. Computational modeling and theoretical analysis of nonlinear fractional order prey–predator system, Fractals 2021, 29, 2150017.
- Moilanen, D.E.; Piletic, I.R.; Fayer, M.D. Water Dynamics in Nafion Fuel Cell Membranes: The Effects of Confinement and Structural Changes on the Hydrogen Bond Network, J. Phys. Chem. C 2007, 111, 8884-8891.
- Goodsell, D.S. The Machinery of Life. Springer Science + Business Media 2009.
- Ninham, B.W.; Bolotskova, P.N.; Gudkov, S.V.; Juraev, Y.; Kiryanova, M.S. etal. Formation of water-free cavity in the process of Nafion swelling in a cell of limited volume; effect of polymer fibers unwinding. Polymers 2020, 12, 2888.
- De Almeida, S.H.; Kawano, Y. Ultraviolet-visible spectra of Nafion membrane. European Polymer Journal 1997, 33, 1307-1311.
- www1.lsbu.ac.uk/water/water_vibrational_spectrum.html
- Yip, J.; Duhamel, J.; Qiu, X.P.; Winnik, F.M. Fluorescence studies of a series of monodisperse telechelicα,ω-dipyrenyl poly(N-isopropylacrylamide)s in ethanol and in water. Can. J. Chem. 2011, 89, 163.
- Holappa, S.; Kantonen, L.; Anderson, T.; Winnik, F.M.; Tenhu, H. Overcharging of Polyelectrolyte Complexes by the Guest Polyelectrolyte Studied by Fluorescence Spectroscopy. Langmuir 2005, 21, 11431.
- Holappa, S.; Kantonen, L.; Winnik, F.M.; Tenhu, H. Self-Complexation of Poly(ethylene oxide)-block-poly(methacrylic acid) Studied by Fluorescence Spectroscopy. Macromol. 2004,37, 7008.
- Miyazawa, K.; Winnik, F.M. Isothermal titration calorimetry and fluorescence spectroscopy studies of the interactions between surfactants and a phosphorylcholine-based polybetaine, in Aqueous Polymer — Cosolute Systems, Progress in Colloid and Polymer Science. Springer, Berlin, Heidelberg 2003, 122, 149–156.
- Mizusaki, M.; Morishima, Y.; Winnik, F.M. An assessment by fluorescence spectroscopy of the stability of polyanions/positively charged liposome systems in the presence of polycations. Polymer 2001,42, 5615.
- https://opentextbc.ca/introductorychemistry/back-matter/appendix-standard-reduction-potentials-by-value-2/
- Eizenberg, D; Kauzmann, W. The Structure and Properties of Water. Oxford Univ., Oxford 1969.
- Alheshibri, M.; Qian, J., Jehannin, M.; Craig, V. S. J. A history ofnanobubbles. Langmuir 2016, 32, 11086–11100.
- Berne, B.J.; Pecora, R. Dynamic light scattering.Krieger, Malabar, Florida, 1990.
- Bunkin, N.F.; and Bunkin, F.V. Bubston structure of water and electrolyte aqueous solutions. Phys. Usp. 2016, 59, 846–865.
- Bunkin, N. F.; Shkirin, A. V.; Suyazov, N. V.; Babenko, V. A.; Penkov, N. V.; Belosludtsev, K. N.; et al. Formation and dynamics of ion-stabilized gas nanobubbles in the bulk of aqueous NaCl solutions. J. Phys. Chem. B 2016, 120, 1291–1303.
- Yurchenko, S.O.; Shkirin, A.V.; Ninham, B.W.; Sychev, A.A.; Babenko, V.A.; Penkov, N.V.; et al. Ion-specific and thermal effects in the stabilization of the gas nanobubble phase in bulk aqueous electrolyte solutions. Langmuir 2016, 32, 11245–11255.
- Uchida, T.; Liu, S.; Enari, M.; Oshita, S.; Yamazaki, K.;Gohara, K. Effect of NaCl on the Lifetime of Micro- and Nanobubbles, Nanomaterials 2016, 6, 31.
- Zhang, H.; Guo, Z.; Zhang, X. Surface enrichment of ions leads to the stability of bulk nanobubbles, Soft Matter 2020, 16, 5470-5477.
- Hewage, S.A.; Kewalramani, J.; Meegoda, J.N. Stability of Nanobubbles in Different Salts Solutions, Colloids and Surfaces A 2021, 609,125669
- Babenko, V.A.; Bunkin, N.F.;Sychev, A.A.Role of gas nanobubbles in nonlinear hyper-Raman scattering of light in water, JOSA B2020, 37, 2805-2814.
- Bunkin, N.F.; Shkirin, A.V.; Penkov, N.V.; Goltayev, M.V.; Ignatiev, P.S.; Gudkov, S.V.; Izmailov, A.Yu. Effect of Gas Type and Its Pressure on Nanobubble Generation, Frontiers in Chemistry 2021, 9, 630074.
- Kelsall, G.H.; Tang, S.Y.; Yurdakul, S.; Smith, A.L. Electrophoretic behaviour of bubbles in aqueous electrolytes, J. Chem. Soc. Faraday Trans. 1996, 92, 3887–3893.
- Takahashi, M. Zeta potential of microbubbles in aqueous solutions: Electrical properties of the gas-water interface. J. Phys. Chem. B2005, 109, 21858–21864.
- Ushikubo, F.Y.; Enari, M.; Furukawa, T.; Nakagawa, R.; Makino, Y.; Kawagoe, Y.; Oshita, S. Zeta-potential of Micro- and/or Nano-bubbles in Water Produced by Some Kinds of Gases, IFAC Proceedings Volumes 2010, 43, 283-288.
- Bunkin, N. F.; Suyazov, N.V.; Shkirin, A.V.; Ignatiev, P.S.; Indukaev, K.V. Nanoscale structure of dissolved air bubbles in water as studied by measuring the elements of the scattering matrix, J. Chem. Phys. 2009, 130, 134308.
- Bunkin, N.F.; Shkirin, A.V.; Kozlov, V.A. Cluster Structure of Dissolved Gas Nanobubbles in Ionic Aqueous Solutions, J. Chem. Eng. Data 2012, 57, 2823-2831.41.
- Bunkin, N.F.; Shkirin, A.V.; Ignatiev, P.S.; Chaikov, L.L.; Burkhanov, I.S.; Starosvetskiy, A.V. Nanobubble clusters of dissolved gas in aqueous solutions of electrolyte. I. Experimental proof, J. Chem. Phys. 2012, 137, 054706.
- Bunkin, N.F.; Shkirin, A.V. Nanobubble clusters of dissolved gas in aqueous solutions of electrolyte. II. Theoretical interpretation, J. Chem. Phys. 2012, 137, 054707.
- Terao, T.; Nakayama, T. Charge inversion of colloidal particles in an aqueous solution: Screening by multivalent ions, Phys. Rev. E 2001, 63, 041401.
- Wang, Z.Y.; Ma, Y.Q. Monte Carlo determination of mixed electrolytes next to a planar dielectric interface with different surface charge distributions, J. Chem. Phys. 2009, 131, 244715.
- Wang, Z.Y.; Ma, Y.Q. Insights from Monte Carlo simulations on charge inversion of planar electric double layers in mixtures of asymmetric electrolytes, J. Chem. Phys.2010, 133, 064704.
- Bunkin, N.F.; Shkirin,A.V.; Suyazov, N.V.; Starosvetskiy, A.V. Calculations of Light Scattering Matrices for Stochastic Ensembles of Nanosphere Clusters,J. of Quant. Spectr. & Rad. Trans.2013, 123, 23–29.
- Jullien, R. Aggregation phenomena and fractal aggregates, Cont. Phys.1987, 28, 477-493.


 Назад
Назад


